查看更多

 明星产品
明星产品
 干货推荐
干货推荐
 关注我们
关注我们

扫码关注我们
了解更多信息
急性缺血性中风是血液发生循环障碍的脑部疾病,是全球范围内导致残疾和死亡的主要原因之一,其特征表现为脑血流中断,引起线粒体代谢障碍。低密度脂蛋白受体相关蛋白(LRP1)作为一种多功能的跨膜受体,它在神经退行性病变等多种疾病中具有重要的生物学功能,这提示着LRP1参与了脑组织的功能调节。尽管LRP1与缺血性中风相关性的研究日益增多,但确切机制尚不明确。据报道星形胶质细胞可通过传递健康线粒体来保护受损神经元,那么LRP1是否也通过调控这一过程来保护缺血性中风的脑组织亟待验证,下面我们介绍一篇关于该机制的最新研究成果。

2024年6月20日,西南医科大学附属医院神经外科江涌教授联合四川大学华西医院李涛教授和中国科学技术大学曹洋教授在《Cell Metabolism》(IF=27.7)上发表题为“Astrocytic LRP1 enables mitochondria transfer to neurons and mitigates brain ischemic stroke by suppressing ARF1 lactylation”的研究论文。本文探讨了LRP1在脑缺血性中风中的保护机制,重点阐明LRP1是如何参与星形胶质细胞向神经元转移线粒体的过程。本文使用星形胶质细胞与神经元共培养的细胞模型和脑中动脉闭塞(MCAO)小鼠模型进行分析,发现星形胶质细胞中LRP1的缺失会抑制其线粒体向受损神经元转移,并加重脑缺血再灌注(I/R)损伤,表明LRP1在缺血性中风中可以起到保护作用。接着作者通过代谢组学、基因表达调控、同位素示踪等方法探索其中的机制。结果发现,在星形胶质细胞中,LRP1通过减少葡萄糖摄取、糖酵解和乳酸的产生,以抑制ADP-核糖基化因子1(ARF1)乳酸化,进而促进星形胶质细胞中健康线粒体转移至神经元中,改善小鼠脑I/R损伤。本研究揭示了LRP1可能成为缺血性中风的一个潜在治疗靶点,为急性缺血性中风治疗研究提供新的思路。
本研究中,汉恒生物有幸为作者提供了LRP1、LDHA/B基因干扰慢病毒以及mito-eRFP-3×flag线粒体标记慢病毒,以实现星形胶质细胞中目的基因的干扰和线粒体标记;此外,本文中使用的CCK-8试剂盒、转染试剂LipoFiter3.0和RNAfit也由汉恒生物提供。
下面我们一起来看看作者是如何发掘其中的机制:
1. 星形胶质细胞中LRP1的缺失会减少其与神经元之间的线粒体转移
作者首先使用mito-eRFP-3×flag慢病毒标记星形胶质细胞中的线粒体,并将其与神经元共培养,验证了星形胶质细胞可以释放线粒体到胞外并转移到神经元中。随后,下调小鼠星形胶质细胞中LRP1基因的表达,发现敲低LRP1后细胞外的线粒体数量减少,并出现功能下降、向神经元转移的能力减弱(图1A-H)。结果表明,星形胶质细胞中的LRP1可促进线粒体向相邻的神经元转移。为了探讨LRP1介导的线粒体转移是否对急性神经元死亡有影响,作者建立了I/R损伤细胞模型,即将HT22神经元与对照或敲低LRP1的星形胶质细胞共培养,在进行2 h的氧糖剥夺(OGD)后再复氧18 h。结果发现,对照组星形胶质细胞保护了神经元免受急性应激损伤,而LRP1敲低组神经元受损(图1 I,J)。以上结果表明,星形胶质细胞LRP1缺失不仅减少了线粒体转移,还会导致神经元对急性应激反应更为敏感。
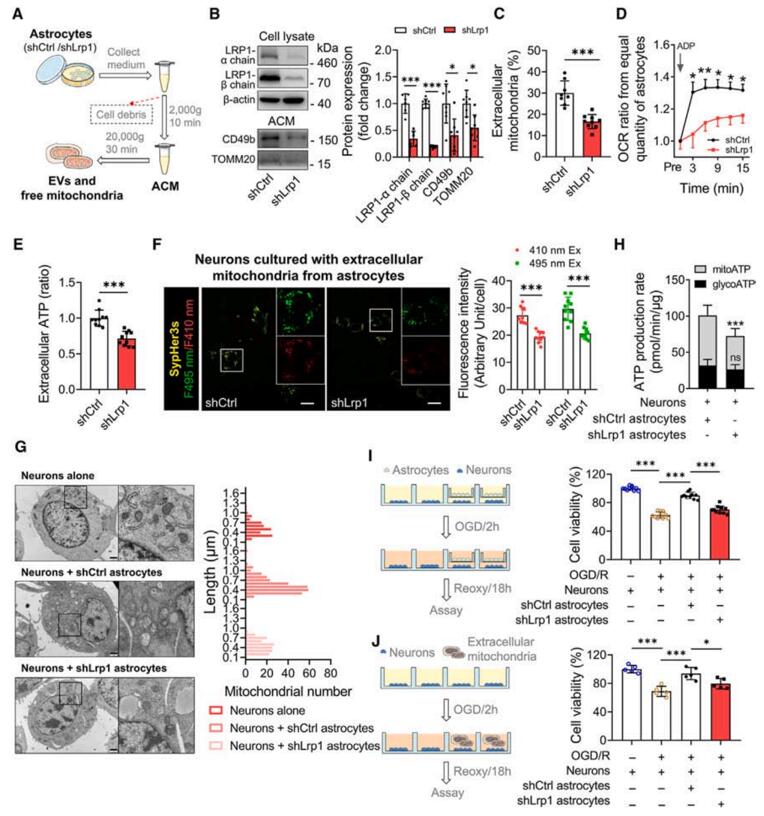
图1. LRP1促进星形胶质细胞向神经元转移线粒体
2. LRP1敲低可增加星形胶质细胞的糖酵解和乳酸生成
接着,作者为了研究LRP1介导线粒体转移的机制,将对照和LRP1敲低的星形胶质细胞进行了靶向代谢组学分析。结果显示,LRP1敲低的星形胶质细胞中胞内的葡萄糖、糖酵解中间产物(3-磷酸甘油醛和乳酸)以及TCA循环中间产物显著增加,表现为糖酵解增强,包括OCR、细胞外酸化率(ECAR)、ECAR/OCR比值上升,LDH活性和LDHA/B亚型增加,以及磷酸果糖激酶(PFK)和丙酮酸激酶(PK)水平升高(图2 A-I)。此外,同位素标记的葡萄糖([U-13C])实验显示,LRP1敲低增加了葡萄糖摄取,并促进了乳酸的生成。结果表明,LRP1敲低后会增加星形胶质细胞对葡萄糖的摄取,增强糖酵解并产生大量乳酸。
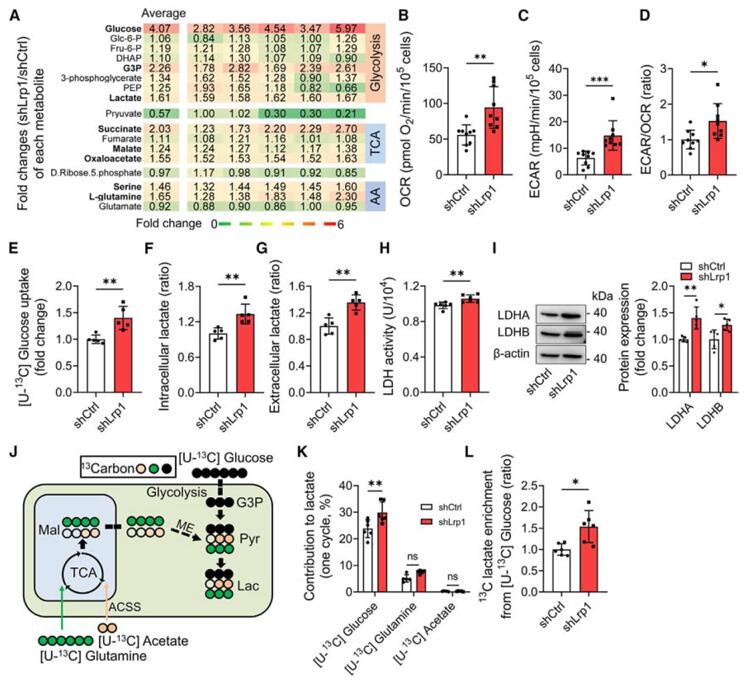
图2. 敲低LRP1可促进星形胶质细胞中的糖酵解和乳酸生成
3. 乳酸抑制星形胶质细胞释放功能性线粒体
因此,作者进一步研究乳酸生成增加对星形胶质细胞释放线粒体的影响。在缺氧条件下,星形胶质细胞中乳酸生成增加,同时细胞外线粒体和ATP水平下降(图3 A,B);反之,用糖酵解抑制剂2-DG处理后,则观察到与上述相反的结果(图3 C)。由于LDH可催化乳酸生成,使用LDH抑制剂(R)-GNE-140 或敲低LDHA/B,得到了与2-DG处理的相同结果,补充乳酸后又逆转了这种效应(图3 D,E)。此外,敲低LDHA/B解除了LRP1敲低对线粒体释放的抑制,而过表达LDHA/B重现了LRP1敲低的效果(图3 F,G)。随后,作者发现乳酸以剂量依赖性方式抑制了线粒体的释放和ATP的生成(图3 H)。以上结果表明,LRP1通过抑制星形胶质细胞中乳酸生成来促进线粒体的释放。
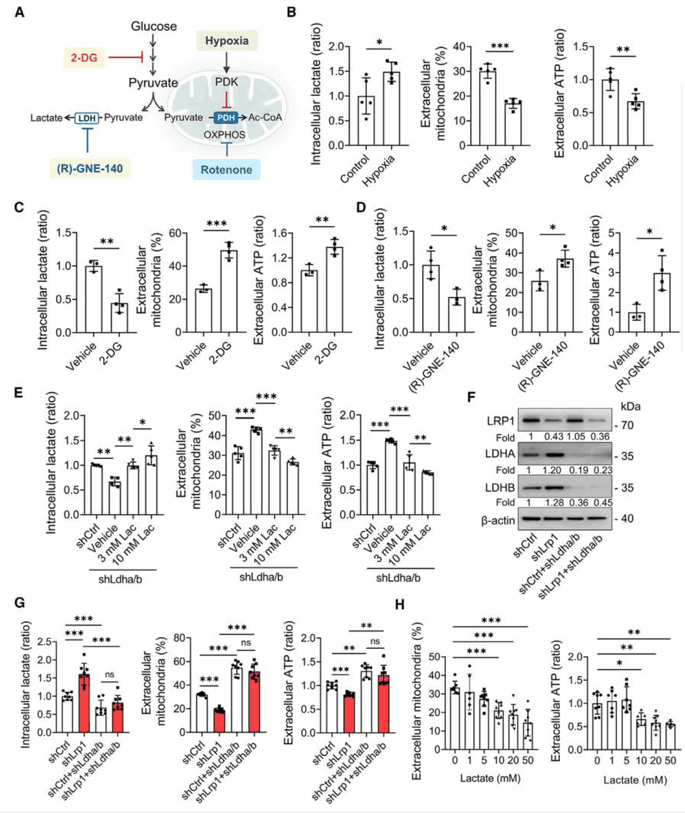
图3. 乳酸抑制星形胶质细胞释放功能性线粒体
4. ARF1-K73乳酸化抑制LRP1诱导的线粒体释放
作者发现,在LRP1敲低的星形胶质细胞中,蛋白质赖氨酸乳酸化(Kla)水平升高,这与乳酸增加的结果相吻合(图4 A)。进一步的乳酸组学分析鉴定出了136种蛋白质具有Kla修饰,其中84种位于细胞核,32种位于细胞质中(图4 B)。由于乳酸增加可快速抑制线粒体转移,推测这种效应可能由细胞质中的乳酸化蛋白介导,其中ARF1的73位赖氨酸(K73)显示出了较高的乳酸化水平(图4 C-E)。实验证实乳酸可诱导ARF1的Kla73修饰,并且ARF1-Kla73与LRP1在功能上有高度相似性(图4 F)。蛋白质互作网络分析表明ARF1 及其相关蛋白在囊泡运输过程中高度富集,提示它们可能参与调控线粒体的释放(图4 G-H)。通过构建ARF1的K73R和K73Q突变体来模拟去乳酸化和乳酸化,发现K73R突变减弱了ARF1的活性并促进了线粒体释放,而K73Q突变则出现相反的效果(图4 I-K)。这些结果表明,ARF1-Kla73是乳酸抑制星形胶质细胞线粒体释放的关键调节因子。
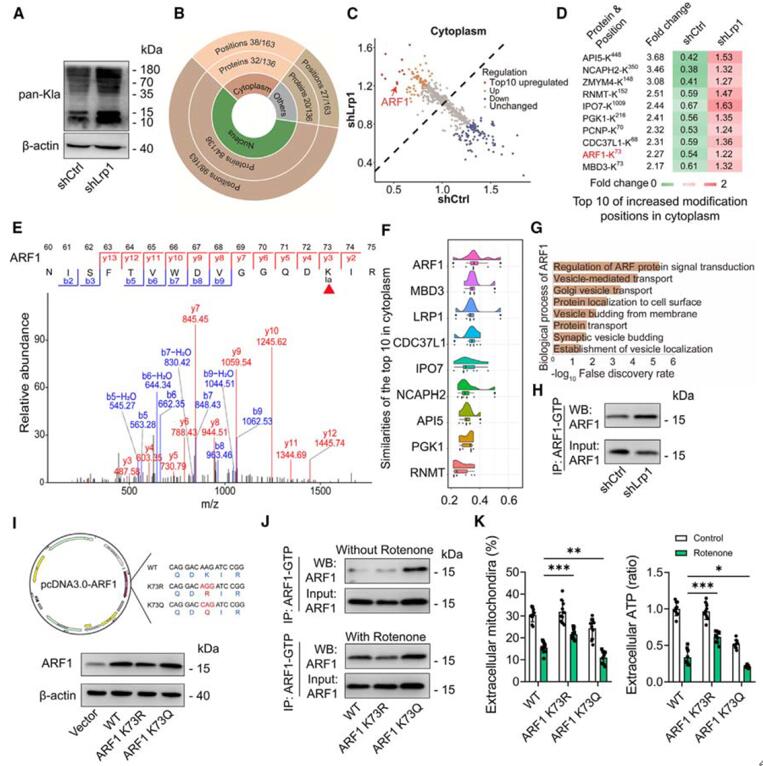
图4. ARF1-K73乳酸化抑制LRP1诱导的线粒体释放
5. LRP1调节线粒体转移可防止脑 I/R 损伤
接下来,作者探究了LRP1诱导的线粒体转移是否能防止脑缺血损伤。作者通过腺相关病毒(AAV2-GfaABC1D-shLRP1)敲低了小鼠大脑中星形胶质细胞中LRP1的表达水平(图5 A)。与对照组相比,LRP1敲低组小鼠表现出葡萄糖摄取增加和脑内乳酸水平升高,这导致脑脊液中星形胶质细胞来源的线粒体减少,且向神经元的转移也减少(图5 B-E)。随后,对小鼠大脑进行MCAO手术以诱发脑I/R损伤。术后发现,LRP1敲低组小鼠的脑梗面积显著扩大、神经功能出现恶化、边界区神经元内的线粒体(尤其是来自星形胶质细胞的线粒体)减少(图5 F-J)。以上结果表明,LRP1通过促进星形胶质细胞线粒体向神经元的转移来防止脑缺血损伤。
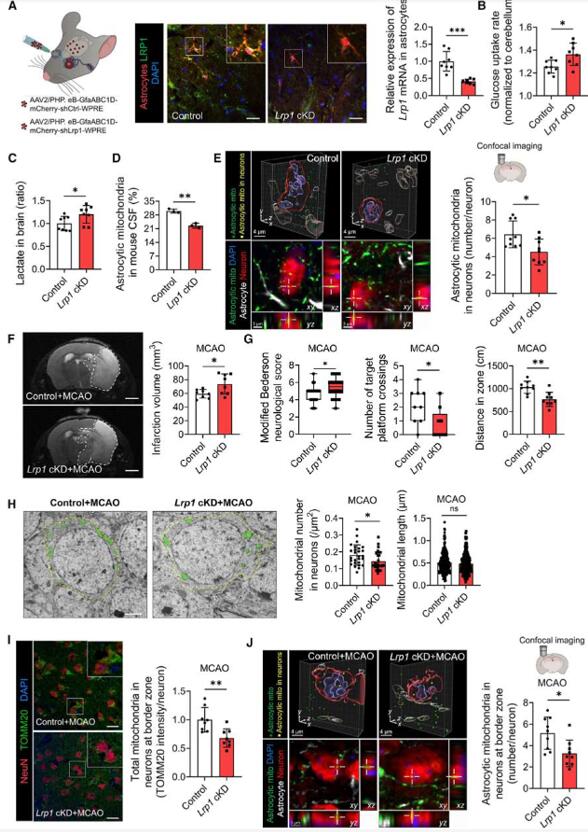
图5. LRP1调控的星形胶质细胞线粒体转移可减轻脑I/R损伤
6. 星形胶质细胞中ARF1-K73乳酸化抑制了线粒体转移,并加重脑 I/R 损伤
作者通过在星形胶质细胞特异性敲低LRP1的小鼠中过表达野生型(WT)ARF1、K73R或K73Q突变体,研究了ARF1-K73乳酸化是否介导了LRP1对脑I/R损伤的保护作用。结果显示,与过表达ARF1-WT的小鼠相比,过表达ARF1 K73R的小鼠脑脊液和神经元中的星形胶质细胞源性线粒体增多,而过表达ARF1 K73Q的小鼠则表现出相反的趋势(图6 A,B)。接着,在MCAO诱发的脑I/R模型小鼠中发现,ARF1 K73R组小鼠表现出较小的脑梗面积、神经功能得到改善,而ARF1 K73Q组则相反(图6 C-F)。此外,在临床中风患者中也检测到了相似的结果(图6 H-J)。这些结果表明,星形胶质细胞中ARF1-K73的乳酸化会减少线粒体转移并加重大脑I/R损伤。
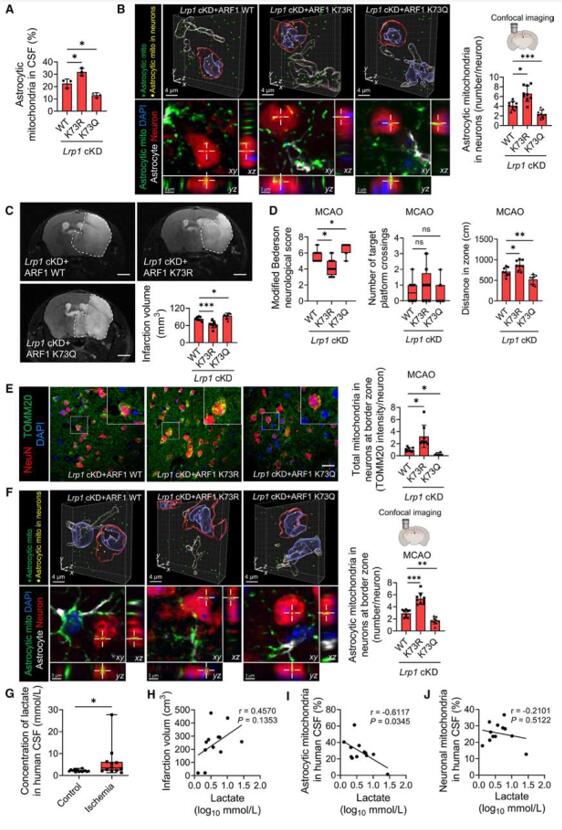
图6. 星形胶质细胞ARF1-K73乳酸化减少了线粒体转移并加重脑 I/R 损伤
综上所述,本研究发现LRP1通过减少乳酸产生和ARF1的乳酸化,促进健康的线粒体从星形胶质细胞向受损神经元中转移,从而在脑缺血性中风中发挥着保护作用。
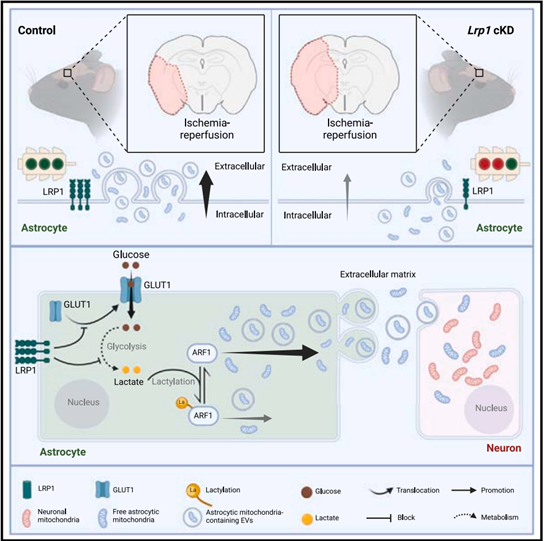
图7. LRP1保护脑I/R损伤的机制示意图

查看更多

查看更多

查看更多

联系我们

返回顶部